La química inorgánica se encarga del estudio integrado de la
formación, composición, estructura y reacciones químicas de los elementos y
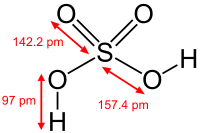
compuestos inorgánicos (por ejemplo, ácido sulfúrico o carbonato cálcico); es decir,
los que no poseen enlaces carbono-hidrógeno, porque éstos pertenecen al campo
de la química orgánica. Dicha separación no es siempre clara, como por ejemplo
en la química inorgánica que es una superposición de ambas. Antiguamente se
definía como la química de la materia inorgánica, pero quedó obsoleta al
desecharse la hipótesis de la fuerza vital, característica que se suponía
propia de la materia viva que no podía ser creada y permitía la creación de las
moléculas orgánicas. Se suele clasificar los compuestos inorgánicos según su
función en ácidos, bases, óxidos y sales, y los óxidos se les suele dividir en
óxidos metálicos (óxidos básicos o anhídridos básicos) y óxidos no metálicos
(óxidos ácidos o anhídridos ácidos)